Aufgrund hoher Inzidenzen der Arthritiden und progredienter Destruktionen, trotz frühestmöglichem Einsatz hochwirksamer Basistherapeutika in modernen Therapiekonzepten, sind schwerwiegende Deformierungen und resultierende Funktionsverluste im Bereich der Hand ein noch immer häufiges Problem für Patienten mit rheumatischen Erkrankungen. Die modernen rekonstruktiven Verfahren der Rheumahandchirurgie erlauben heute auch langfristig eine gute Schmerzfreiheit, Funktion und Ästhetik der Hand des Rheumapatienten zu erhalten.
Rheumatische Handdeformität
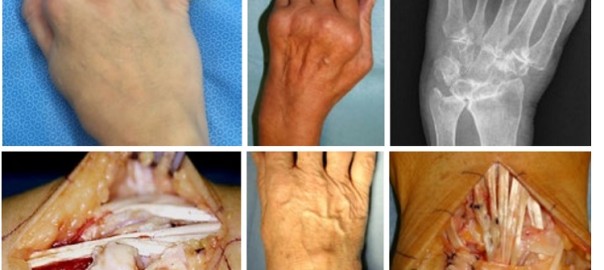
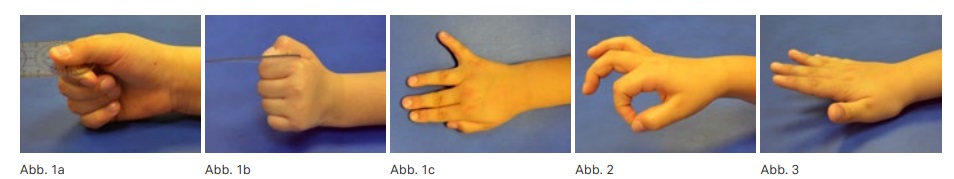
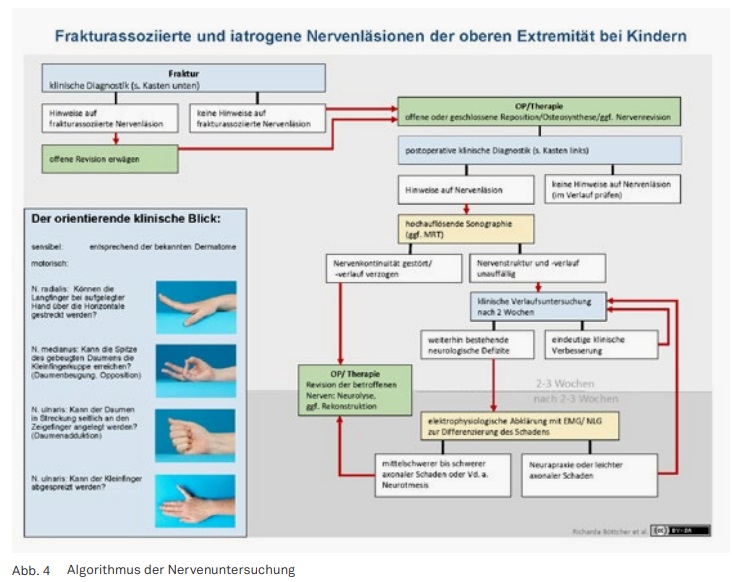
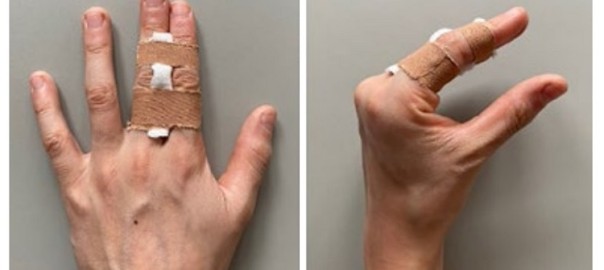
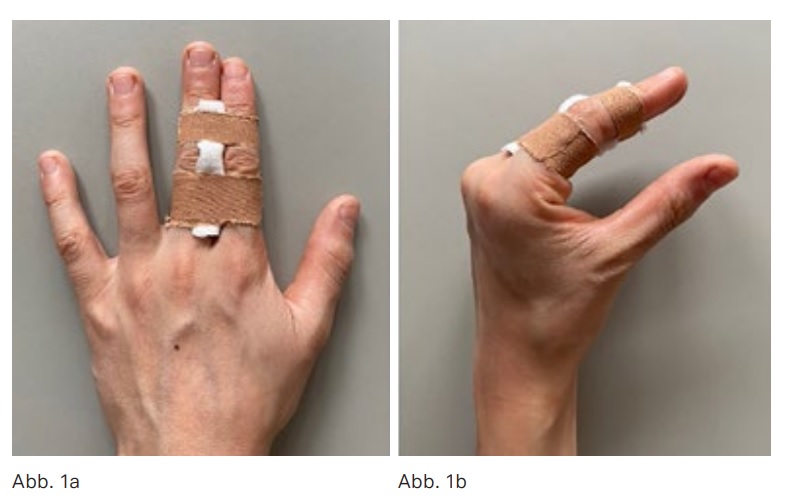
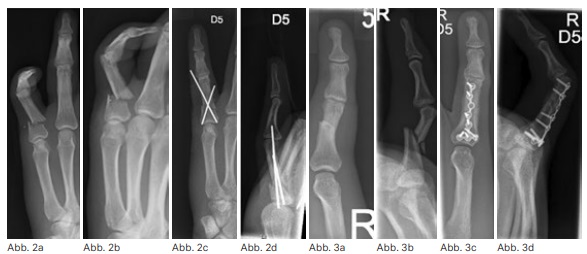
Die charakteristischen Veränderungen der Hand bei den verschiedenen rheumatischen Erkrankungen sind zahlreich (Rheumatoide Arthritis (RA) und Psoriasisarthritis haben wegen der Häufigkeit der destruierenden Folgen eine besondere Bedeutung, die Hand ist aber auch bei den Spondyloarthritiden, Kollagenosen etc. oft betroffen) und für die Patienten meist mit Funktionsverlusten, Schmerzen sowie stigmatisierenden Fehlstellungen verbunden. Die Komplexität der Handanatomie führt zu unterschiedlichen typischen Läsionsmustern rheumatischer Erkrankungen, mit knöchernen Erosionen, Destruktionen der intrinsischen und extrinsischen Bandsysteme, Kapseldeformierungen sowie Sehnen- und Sehnengleitgewebsläsionen. (Abb. 1) Zu beachten sind besonders die rheumatische Handdeformität („Handskoliose“ mit Supinationsfehlstellung und Ulnartranslokation des Karpus, Ulnardeviation der dreigliedrigen Finger) und das Caput-ulnae-Syndrom (palmare Subluxation des Radius und ulnaren Karpus gegenüber dem dorsal prominenten Ulnakopf mit Risiko der Strecksehnenruptur). Die verlorene Hand- und Handgelenksfunktion bedeutet für den Betroffenen oft eine schwerere Behinderung als der Verlust der Gehfähigkeit, da eine Selbstversorgung fast unmöglich werden kann. (Abb. 2–4)
Behandlungskonzept Rheumahandchirurgie
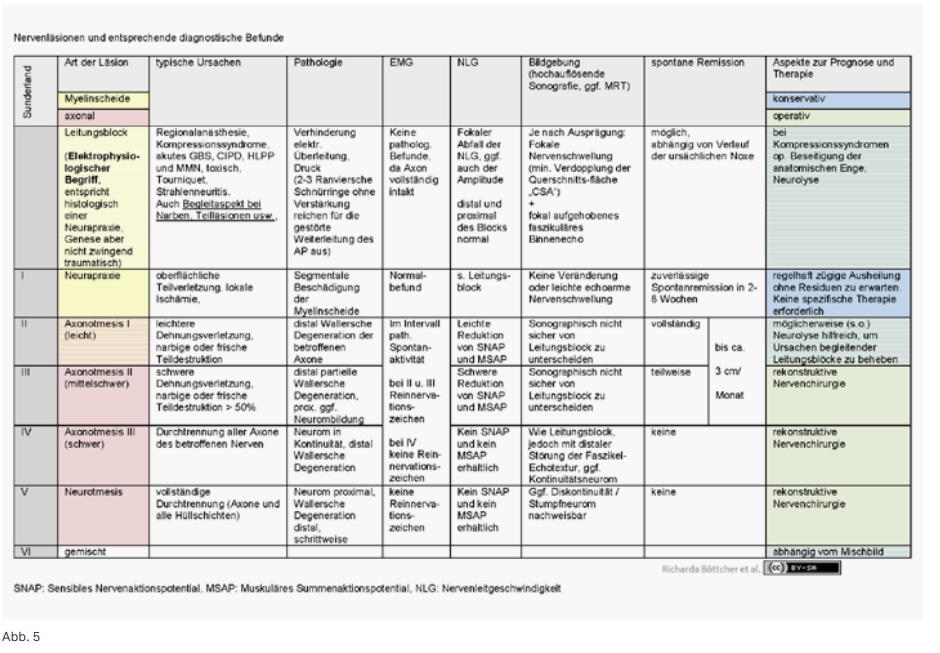
Bei den operativen Therapien kann unterschieden werden zwischen präventiven (z. B. Synovialektomien) und rekonstruktiven Maßnahmen (z. B. Sehnenrekonstruktion, Gelenkersatz). Obwohl die Anzahl vor allem der präventiven Eingriffe bei Patienten mit rheumatischen Erkrankungen, aufgrund der modernen medikamentösen Therapieformen, in den rheumahandchirurgischen Zentren zurückgeht, ist doch häufig eine operative Therapie der Hand erforderlich. Nicht nur bei den „silent Progressions“ (Voranschreiten der arthritischen Destruktionen ohne Schmerzen und Entzündungsparameter), unbehandelten bzw. unzureichend behandelten Patienten, Infektionen oder deren Folgen, sondern auch im Verlauf länger bestehender Erkrankungen bei suffizienter medikamentöser Behandlung, werden zunehmend rekonstruktive rheumahandchirurgische Therapien notwendig. Persistierende Synovialitiden besonders des 6. Strecksehnenfaches sind häufig mit einem operativen Therapiebedarf verbunden. Das Behandlungskonzept resultiert dann aus dem Patientenbedarf (Einschränkungen im Alltag, Behandlungswunsch), der klinischen und bildgebenden Befunde (z. B. Standardröntgentafeln nach Larsen, Dale und Eek) sowie der Verlaufserwartung der Erkrankung im Bereich der Hand (z. B. „natürliche“ 3 Verlaufstypen (ankylosierender, sekundär osteoarthrotischer, desintegrativer Typ) am Handgelenk bei der RA). (Abb. 5)
Operative Therapie am rheumatischen Handgelenk
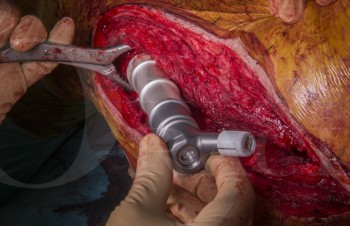
Synovialektomie (=Entfernung der Gelenk-/peritendinösen Schleimhaut): Die präventive Synovialektomie erfolgt bei geringen Destruktionen mit persistierender Synovialitis trotz adäquater Basistherapie. Sie ist regelhaft bei den rekonstruktiven Maßnahmen (Spätsynovialektomie) gleichzeitig durchzuführen.
Die arthroskopische Synovialektomie des Handgelenks bei artikulären Synovialitiden ohne Tenosynovialitis hat ein geringeres Gewebetrauma und schnellere Rehabilitation. Die offene Arthrosynovialektomie erfolgt vor allem bei gleichzeitiger Tenosynovialitis. Die Subkutanverlagerung der Strecksehnen, wenn notwendig Ulnakopfresektion
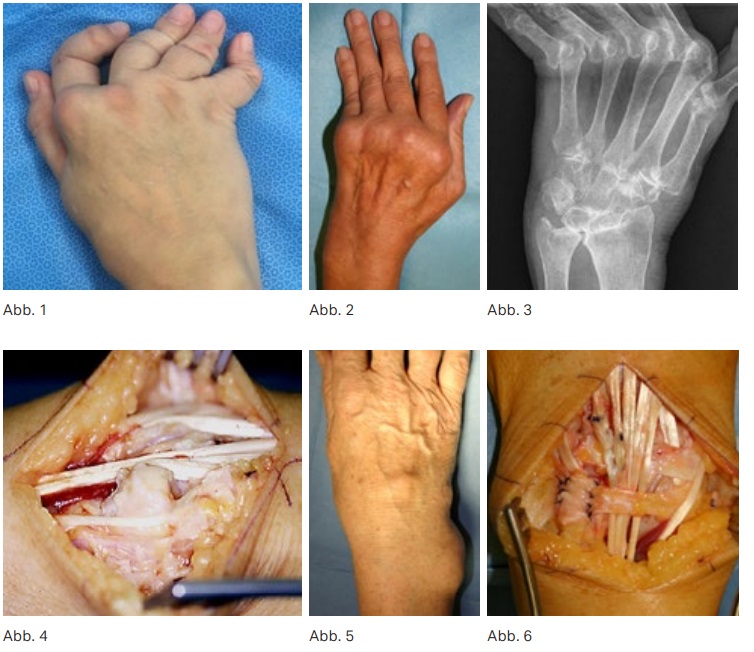
und die radiokarpale Stabilisierung durch die „Dorsal wrist stabilization“ (Transposition des Retinaculum ext. unter die Strecksehnen und ulnare Fixation am Karpus) sowie die Reposition der Sehne des M. ext. carpi ulnaris nach dorsal und Stabilisierung mittels des Retinaculum werden häufig kombiniert. (Abb. 6)
Ulnakopfresektion
Die Ulnakopfresektion ist nicht generell Bestandteil der Handgelenkssynovialektomie. Ist der Ulnakopf überwiegend destruiert und ein Caput-ulnaeSyndrom vorliegend kommt aber die Resektion mit weichteiliger Stabilisierung des distalen Ellenstumpfes in Betracht. Kann mit Weichteileingriffen keine Stabilisierung erreicht werden, muß, in Abhängigkeit vom Stadium der Destruktion und Knorpelsituation, eine knöcherne Fixierung erfolgen.
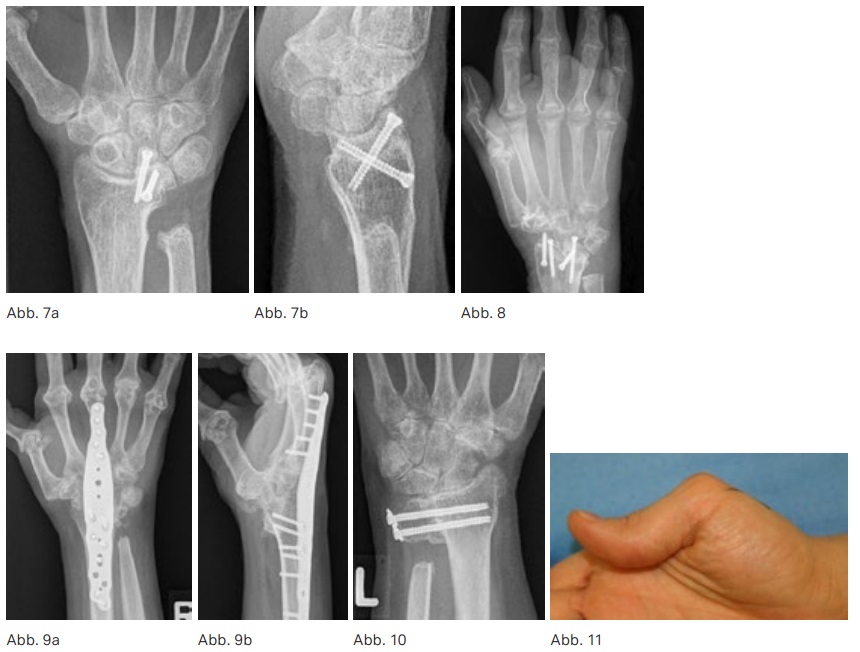
Radiolunäre Fusion Die radiolunäre Arthrodese führt zur Stabilisierung des Handgelenkes in der frontalen und sagittalen Ebene bei erhaltener und im präoperativen Vergleich nur gering eingeschränkter Handgelenksbeweglichkeit. Sie ist indiziert bei intaktem radioskaphoidalem sowie mediokarpalem Gelenk, ggf. mit gleichzeitiger Resektion des Ulnakopfes. (Abb. 7a & b)
Radioskapholunäre Fusion
Radioskapholunäre (RSL) Arthrodesen sind indiziert bei fortgeschrittenen Destruktionen des radioskaphoidalen und radiolunären Gelenkes, aber erhaltenem Knorpel des Mediokarpalgelenkes. Das erreichbare Bewegungsausmaß ist geringer als bei der radiolunären Fusion. (Abb. 8)
Arthrodese
Ausgeprägte Handgelenksdestruktionen mit radiokarpalen und mediokarpalen (evtl. auch karpometakarpalen) Knorpeldefekten (ggf. auch Instabilität) erfordern die Arthrodese. Auch bei Rupturen der Handgelenksstrecksehnen ohne Rekonstruierbarkeit und nach fehlgeschlagener Endoprothese kommt die Arthrodese in Betracht. (Abb. 9a & b)
Alloarthroplastik
Die Diskussion zur Handgelenksendoprothetik bei Patienten mit rheumatischen Erkrankungen besteht vor allem bei fortgeschrittenen Destruktionen und ankylosierenden Verlaufstypen, die eine beidseitige Handgelenksdestruktion oder einen besonderen Bedarf feinmotorischer Gebrauchsfähigkeit der Hand haben. Es besteht generell für die Handgelenksprothetik bei rheumatischen Erkrankungen eine besondere Belastungssituation mit erhöhtem Risiko der Lockerung und Prothesenmigration,
des Materialbruches und aufgrund des meist gestörten muskulären Kräftegleichgewichtes das Problem der Entstehung einer störenden Sekundärfehlstellung.
Operation nach Kapandji (Sauvé-Kapandji)
Die radioulnare Arthrodese mit Ulnasegmentresektion wird zur operativen Behandlung bei Caputulnae-Syndrom und zur Stabilisierung des Handgelenkes durchgeführt. Ein ausreichend intakter Ellenkopf ist für diese Operation notwendig. Besonders das kosmetische Ergebnis dieser Operation wird von den Patienten meist als besser als das der Ulnakopfresektion empfunden. Ob der Eingriff ähnlich der partiellen radiokarpalen Fusion das rheumatische Handgelenk langfristig stabilisieren kann, wird in der Literatur uneinheitlich bewertet. Auch in Stadien fortgeschrittener Handgelenksdestruktionen ist die Operation oft erfolgreich. (Abb. 10)
Operative Therapie rheumatischer Daumen- und Fingerdeformitäten
Korrektureingriffe bei Ulnardeviation, palmarer Sub-/Luxation der Fingergrund-/mittelgelenke, Schwanenhals- und Knopflochdeformitäten sowie Daumendeformitäten können in Abhängigkeit vom Stadium und Typ (z. B. n. Nalebuff) sehr aufwendig und mit umfangreichen Nachbehandlungen verbunden sein. Oft sind auch heute Rekonstruktionen bei rheumabedingten Sehnenrupturen notwendig. Die Ergebnisse sind dabei vom Ort der Läsion und Anzahl der betroffenen Sehnen abhängig. Aus der Fülle der verschiedenen Eingriffe an Daumen und Fingergelenken soll nur beispielhaft auf zwei typische rheumahandchirurgische Verfahren eingegangen werden.
Alloarthroplastik und Korrektur der Ulnardeviation
Die Indikation zum Gelenkersatz besteht als rekonstruktive Maßnahme bei fortgeschrittenen Gelenkdestruktionen. Die knöcherne Substanz gerade im Bereich der Mittelhandknochen bei Patienten mit Rheuma ist oft schlecht, die Verankerung von Implantaten dadurch erschwert und eine palmare/ ulnare Fehlstellung liegt vor. Die größten Erfahrungen bestehen weltweit mit dem Silikon-Implantat (z. B. Swanson), das auch heute noch den Gelenkersatz der Wahl im Bereich der Fingergrundgelenke beim Patienten mit RA darstellt. Die Gelenkstabilisierung, Wiederherstellung der Länge des Fingerstrahls, Schmerzreduktion und der Funktionserhalt auch in Knochen schlechter Qualität ist hiermit möglich. Die Synovialektomie, Lösung der palmaren Platte, Reinsertion der radialen Kollateralbänder sowie Rezentrierung der Strecksehne sind Bestandteile der Gelenkersatzoperation und gff. Korrektur der Ulnardeviation. (Abb. 8)
90-90-Deformität des Daumens
Diese ist charakterisiert durch die Beugefehlstellung des Daumens im Grundgelenk mit sekundärer Überstreckung im Interphalangealgelenk. Die Behandlung ist vor allem abhängig vom Zustand der Gelenkflächen. Bei geringen Destruktionen kann die Tenodese nach Nalebuff durchgeführt werden. Nach dem distalen Absetzen wird hier die Sehne des M. ext. pollicis longus durch die dorsale Kapsel des Grundgelenkes an der Basis der Grundphalanx gezogen und vernäht. Die extrinsische Daumenstreckung wird so verstärkt. Ist das Daumengrundgelenk fortgeschritten zerstört, erfolgt die Arthrodese. (Abb. 11)
Rheumahandchirurgie im interdisziplinären Behandlungskonzept des Rheumapatienten
Ohne suffizient und kontrolliert durchgeführte Basistherapie, als zentral-wesentlicher Anteil der Behandlung der Patienten mit einer rheumatischen Erkrankung, kann kein rheumahandchirurgischer Eingriff geplant oder langfristig erfolgreich werden. Diese medikamentöse Einstellung erfolgt regelhaft ambulant, wie auch die weiteren konservativen Therapiemaßnahmen. Rheumahandchirurgische Eingriffe (besonders Handgelenks-, Fingergelenks-, Sehnenoperationen) erfordern hingegen fast immer stationäre postoperative Behandlungen über mehr als 48 Stunden, um das operative Ergebnis nicht zu gefährden und die spezifische rheumahandtherapeutisch-frühfunktionelle Nachbehandlung unter Kontrolle durch den Rheumahandchirurgen zu ermöglichen. Eine enge ambulant-stationäre Verbindung ist dabei nötig. Der Rheumahandchirurg, als Facharzt mit gleichzeitig zwei Zusatzbezeichnungen: orthopädische Rheumatologie und Handchirurgie, ist im interdisziplinären Konzept zusammen mit orthopädischen Rheumatologen, internistischen Rheumatologen, hinzuzuziehenden weiteren Fachärzten und Berufsgruppen ambulant und stationär notwendig. Der Gesetzgeber hat hierfür z. B. mit der ambulanten spezialfachärztlichen Versorgung (ASV) die Grundlage der ambulanten Behandlungsstruktur geschaffen. Der ASV Rheumatologie wird im Krankenhaus Waldfriede Berlin auch bundeslandübergreifend schon seit mehr als einem Jahr gelebt.
Literatur auf Anfrage bei der Redaktion.