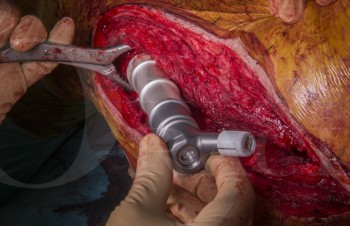
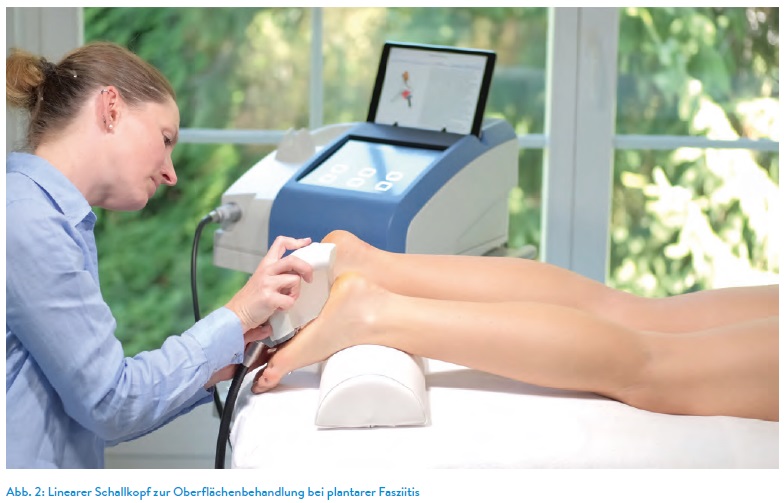
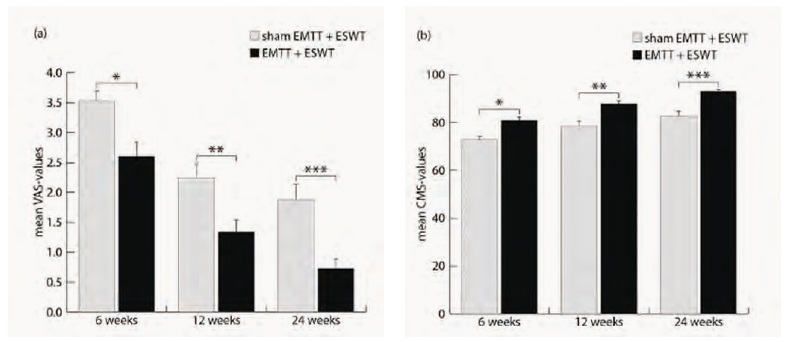
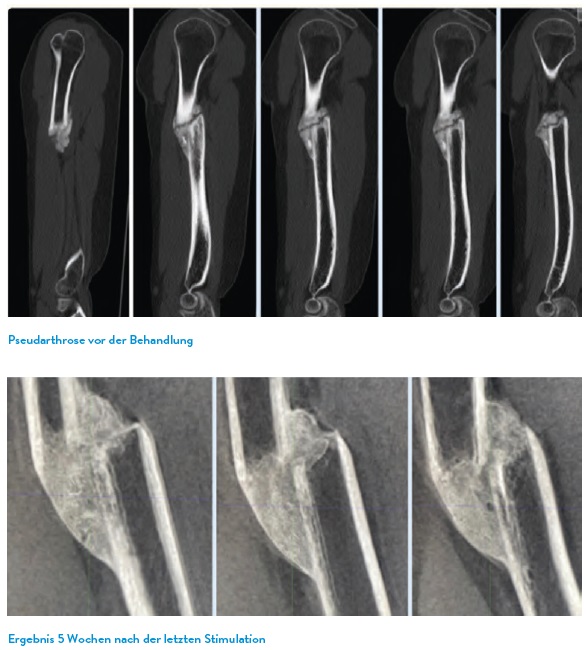
Knorpelveränderung über Zeit und Belastung:
Der Gelenkknorpel unterliegt im Alltag einer ständigen Belastung mit Kompression und Scherkräften, die insbesondere bei begleitenden Instabilitäten des Gelenks zu einer Schädigung des Knorpels führen. Bei einem traumatischen Ereignis kann dies zu einer direkten Schädigung der Gelenkoberfläche führen, während unter Berücksichtigung der multifaktoriellen Genese von Arthrose, Osteochondrosis dissecans und Osteonekrose auch wiederholte Mikrotraumata, genetische Prädispositionen, biomechanische Aspekte bei Gewichtsbelastung durch Adipositas und Achsfehlstellungen zu berücksichtigen sind. Eine weitere Gruppe bilden die chronisch-entzündlichen Veränderungen der Synovia z. B. bei der rheumatoiden Arthritis mit folgender Knorpelschädigung. Es zeigt sich also bei unterschiedlicher Ätiologie eine gleichartige Konsequenz für die betroffenen Gelenke mit Einfluss auf Gelenkfunktion, Bewegungseinschränkung und vom Patienten geäußerter Schmerzsymptomatik. Aufgrund der fehlenden Blutversorgung zeigt sich das regenerative Potential von Knorpelgewebe sehr eingeschränkt.
Wirkungsmechanismen der ESWT:
Die extrakorporale Stoßwellentherapie zeigt seine Wirkung in der medizinischen Anwendung über eine Reihe von biologischen Pfaden, die in der langjährigen Anwendung und Grundlagenforschung nachgewiesen werden konnten. In vielen Bereichen zeigen sich noch eingeschränkte Kenntnisse, und dennoch kann bereits über die Zusammenführung der bekannten biologischen Kaskaden und die nachgewiesenen Effekte haltbare Theorien zur Wirksamkeit aufstellen.
Grundsätzlich lässt sich heute sagen, dass die Anwendung der extrakorporalen Stoßwellenapplikation bei muskuloskelettalen Verletzungen als regenerative Medizin verstanden werden kann.
Bei dieser nicht-invasiven Therapieform werden Wachstumsfaktoren freigesetzt und biologische Gewebsreaktionen im behandelten Areal hervorgerufen. Bekannte Effekte in der medizinischen Anwendung sind die Schmerzlinderung, Verbesserung der Blutversorgung, Proteinsynthese und Zellproliferation und damit die Grundlage einer Stimulation der körpereigenen regenerativen Fähigkeiten.
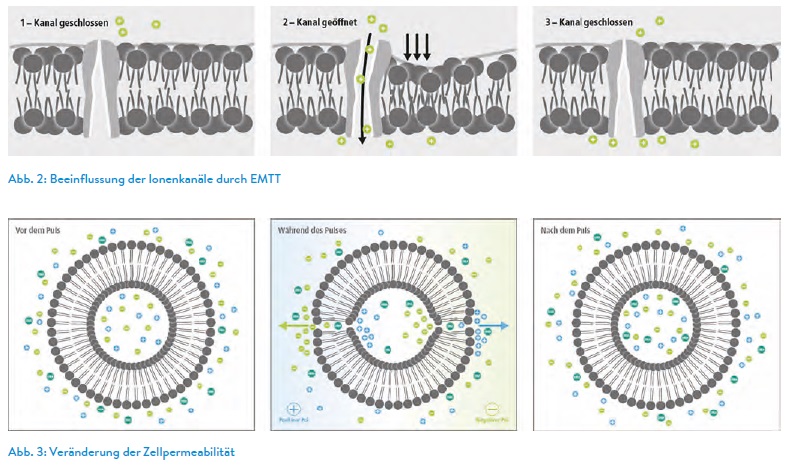
Wirkung der Mechanotransduktion auf biologische Gewebe: Als Wirkmechanismus hat sich das Prinzip der Mechanotransduktion durchgesetzt. Mechanotransduktion wird in drei wesentliche Anteile unterschieden.1 Ein Netzwerk von Proteinen, Ionen-Kanälen und Lipiden vermittelt dann die zu erzielende Wirkung.
Zunächst das „mechanocoupling“, dem physikalischen Einwirken der mechanischen Kräfte auf die behandelten Zellen mit einer kurzzeitigen Verformung des Gewebes, was über Scher- und Druckkräfte zu einer Störung der Zelle und chemischen Reaktionen innerhalb der Zelle aber auch zwischen den kommunizierenden Zellen führt.
Die Auswirkung auf die Zell-zu-Zell-Kommunikation gilt als zweiter Anteil der Mechanotransduktion, bei der es zu einer Wirkungsausbreitung vom behandelten Areal durch die Ausbreitung von Calcium (Ca2+) und Inositol-Triphosphat (IP3) über Gap-junctions auf das gesamte zu behandelnde Gewebe kommt. Auf diese Weise erreicht der mechanisch eingebrachte Stimulus der ESWT auch Zellen im anliegenden Gewebe, die nicht direkt behandelt werden.
Als dritten Anteil wird die zelluläre Antwort der behandelten Zellen gesehen. Hierbei wird durch die mechanische Einwirkung der energiereichen Stoßwellen eine Zug- und Druckkomponente auf das Zielgewebe ausgelöst, die an den Grenzschichten von extrazellulärer Matrix und Zelle zur Auslenkung der ortsständigen Integrine führt. An diesem Punkt wird über die mechanische Einwirkung eine biologische Reaktion erwirkt, die zur Gewebereparatur und -regeneration führt. Zum einen kommt es über die Einbindung des Zytoskeletts zur direkten physikalischen Kommunikation mit dem Zellkern. Begleitend erfolgt über die Aktivierung der Integrine eine biochemische Signalkettenaktivierung mit Einfluss auf die Genaktivierung im Zellkern, was zur Freisetzung von mRNA in das endoplasmatische Retikulum und die Proteinsekretion in die extrazelluläre Matrix führt. Auf diese Weise wird über den mechanischen Stimuluseine Remodellierung der Matrix erreicht.
Wie andere muskuloskeletale Gewebe ist auch das Knorpelgewebe mit mechanosensitiven Zellen besiedelt, die Chondrozyten. Der Knorpel gilt daher als mechanosensitives Gewebe, woraus folgt, dass der Knorpel mechanische Reize wahrnehmen und darauf reagieren kann. In einer Reihe von Forschungsansätzen konnte gezeigt werden, dass die unterschiedlichen Zug- Scher- und Druckkräfte zu unterschiedlichen Wirkungen im Knorpelgewebe führen können und über die Intensität der Einwirkung einen positiv regenerativen oder aber schädigenden Effekt erzielen können.2
Die dynamische Kompression des Knorpels während der physiologischen Nutzung führt über die Veränderung der Synovialflüssigkeit und diffundierenden Bereitstellung von Nährstoffen und Sauerstoff zur Erhaltung des Gelenkknorpels. Begleitend zeigt sich der oben beschriebene Effekt der Genexpression in Chondrozyten. Hierbei konnte gezeigt werden, dass die Genexpression abhängig ist von Stärke, Frequenz und Dauer der Druckeinwirkung. Es konnte gezeigt werden, dass eine dynamische Kompression die Expression anaboler Gene, wie ACAN, COL2A1 und TIMP3 bewirkt, während die Gruppe der Matrix-Metalloproteinasen runterreguliert werden.
Eine sanfte Druckeinwirkung zeigt eine antiinflammatorische Wirkung. Dagegen werden über zu hohe Druckkräfte schädigende Wirkungen gesehen, die wiederum zur Freisetzung von NO, COX2, PGE₂ und MMP1 führen. Neben der Intensität zeigt auch eine anhaltende Dauer einen negativen Effekt auf den Gelenkknorpel.
Über die Zugkräfte werden Inflammation und Reparaturprozesse in Chondrozyten reguliert. Auch hier sind die unterschiedlichen Intensitäten entscheidend über die Auswirkung auf den Knorpel. Sanfte Zugkräfte wirken antiinflammatorisch und inhibieren IL-1β, TNF-α- und Lipopolysaccharid-induzierte proinflammatorische Gentranskriptionen.
Knobloch et al. konnten in ihrem Review über die Einwirkung mechanischer Kräfte auf den Gelenkknorpel zeigen, dass mechanische Stimuli in Abhängigkeit von Intensität, Frequenz und Dauer mal positive, aber auch negativ auf die Knorpelintegrität wirken kann.2
Biologische Effekte der ESWT im Gewebe:
Bei der Anwendung der extrakorporalen Stoßwelle wird die mechanotransduktorische Wirkung in Anlehnung an die Grundlagenforschung von Hohlfeld et al.3 über die Aktivierung von β-1-Integrinen an der Zelloberfläche, die mit intrazellulärer Steigerung von ERK zur Freisetzung von Signalproteinen in sogenannten Exosomen eine interzelluläre Kommunikation ermöglichen, wobei über TLR-3-Rezeptoren eine kurzfristige Inflammationssteigerung mit direkt anschließender Inflammationsreduktion initiiert wird.
Die ESWT zeigt eine Reihe von positiven Effekten im Körper. Stoßwellenapplikation führt zu einer Steigerung des NO-Levels In der Untersuchung am Hautlappen-Modell konnte die Gruppe von Mittermayr et al.4 zeigen, dass die Anwendung der ESWT sowohl als präconditionierende Behandlung, als auch nach erfolgter Unterbrechung der Blutversorgung zu einer signifikanten Steigerung der Durchblutung im beobachteten Hautlappen führten.
Die intensive Untersuchung der Wirkmechanismen der ESWT in der Arbeitsgruppe um Johannes Holfeld5 konnte bei der Anwendung der ESWT am Myokard ebenfalls eine stoßwellenvermittelte Verbesserung der Blutversorgung zeigen. So konnte nachgewiesen werden, dass über die Freisetzung von VEGF und PlGF die Angiogenese, im Sinne einer Gefäßsprossung aus vorhandenen Gefäßen, vermittelt wird.
Weiter konnte auch eine Anlockung und Rekrutierung von aus dem Knochenmark stammenden mesenchymalen Stammzellen (BMSC) über die Bindung von SDF-1 an VEGF mit resultierender Neubildung von Gefäßen im behandelten Gewebe im Sinne der Vasculogenese. Auch Aicher et al.6 zeigten bereits 2006 eine Rekrutierung und Einnistung von i.v.-applizierten Stammzellen durch eine Präkonditionierung des zu behandelnden Gewebes mittels extrakorporaler Stoßwellen.
MSCs, ADSCs und subchondrale Knochenstamm-/Vorläuferstammzellen (SCB-SPCs) sind potenzielle Optionen für die Reparatur von Knorpelgewebe. Es erscheint daher sinnvoll bei der Behandlung von Knorpelläsionen auch die mechanotransduktorischen Potentiale der extrakorporalen Stoßwellentherapie für eine Rekrutierung von benötigten Stammzellen zu nutzen.
Inwieweit die physikalischen Effekte einer Druck- und Zugbelastung auf die Zelle in Ihrer Wirkung durch Anpassung von Frequenz, Intensität und Anzahl der applizierten Stoßwellen für unterschiedliche Gewebetypen eine optimale Zahl zeigen, ist zum aktuellen Zeitpunkt nicht zu sagen. Es zeigt sich aber, dass verschiedene Gewebetypen auch mit unterschiedlichen Intensitäten behandelt werden. So werden aktuell Nervengewebe mit relativ niedrigen Intensitäten bearbeitet, während der Knochen offensichtlich eine deutlich höhere Energieflussdichte benötigt, um eine regenerative Reaktion zu zeigen.
Studienentwicklung zur ESWT am Gelenkknorpel:
Ähnlich zur Beschreibung der zusammengetragenen Ergebnisse im Review von Knobloch et al.2 zeigt sich auch in der Anwendung der ESWT am Gelenkknorpel der Hinweis auf eine wichtige Dosis-Wirkungsbeziehung.
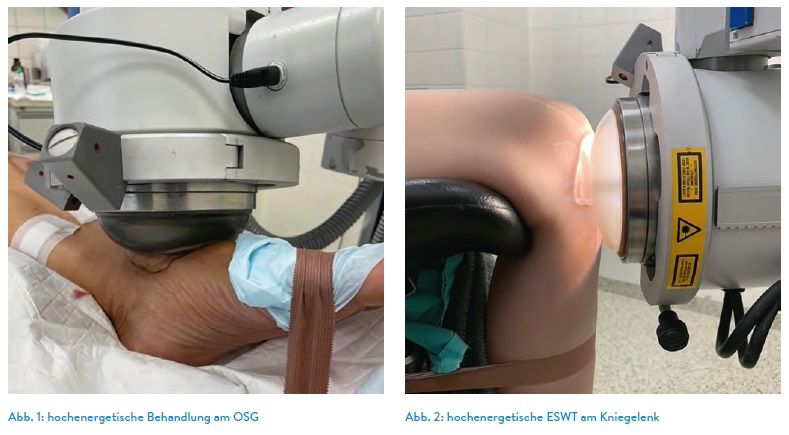
Zhang et al.7 konnten in einer in-vitro-Studie zeigen, dass radiale Stoßwellen die Proliferation und Selbsterneuerung von mesenchymalen Stammzellen in vitro signifikant förderten und den Knorpelreparaturprozess in vivo sicher beschleunigten, was auf günstige klinische Ergebnisse hindeutet. Hierbei zeigte sich insbesondere eine Verbesserung der Oberflächenstruktur des behandelten Knorpelgewebes.
Mayer-Wagner et al.8 zeigten bei der Anwendung von hochenergetischen Stoßwellen auf den hyalinen Knorpel von Ratten eine strukturschädigende Wirkung, wobei hier in einer Einzelbehandlung 1 500 Impulse eine vergleichbar sehr hohe Energieflussdichte von 0,5 mJ/mm2 appliziert wurde. Es zeigte sich eine Reorganisation der Matrixproteine und Erhöhung der COL2A1-mRNA nach der Stoßwellenapplikation.
Wang et al.9 konnten dagegen in ihrer mehrteiligen Studie an Kaninchen zeigen, dass eine Behandlung bei einer induzierten Arthrose ein chondroprotektiver Effekt durch die Stoßwellenbehandlung erzielt werden kann. Dargestellt wurde eine Erhöhung des Typ-2 Kollagens sowie eine signifikante Steigerung von VEGF, BMP-2 und Osteocalcin im subchondralen Knochen. Die positiven Wirkungen von ESWT scheinen ab 4 Wochen nach der Behandlung zeitabhängig zu sein.10
Im Gegensatz zu den Arbeitsgruppen um Mayer-Wagner und Zhang hat in der vorliegenden Untersuchungsreihe von Wang et al.11 die Behandlung im subchondralen Bereich gelegen. Wang konnte hier zeigen, dass die subchondrale Anwendung der ESWT bei einer Arthrose eine ortsspezifische Wirkung am distalen Femur und an der proximalen Tibia erreicht. Die Wirkungen von ESWT sind am distalen Femur und an der proximalen Tibia konsistent, ohne additive Effekte, wenn beide Bereiche gleichzeitig behandelt wurden. In 2013 veröffentlichten Wang et al.12 zudem eine Vergleichsstudie, die zwischen der Behandlung des subchondralen Knochens gegenüber der direkten Behandlung des Gelenkknorpels unterscheidet. Im Gegensatz zur Oberflächenbehandlung des Gelenkknorpels verbesserte eine ESWT am subchondralen Knochen die Geweberegeneration im Verlauf von Arthrose-Veränderungen, wobei sich die Behandlungsparameter nicht unterscheiden. Es wurden sowohl chondral als auch bei der Behandlung des subchondralen Knochens mit 800 Impulsen bei einer Energieflußdichte von 0,25 mJ/mm2 (14 kV) behandelt.
Lyon et al.13 zeigten 2013 in einer Studie an Kaninchen bei der Behandlung der Osteochondrosis dissecans, dass die hochenergetische Behandlung mit 4 000 Impulsen bei 4 Hz und 0,24 mJ/mm2 (18 kV) nach Entnahme einer 4 mm durchmessenden Knorpel-Knochen-Stanze aus der gewichtstragenden Femurkondyle zu einer beschleunigten Knochenheilung, erhöhten Knorpeldichte und subchondralen Knochendichte in der histologischen Nachuntersuchung führte. Die Autoren kommen zu der Schlussfolgerung, dass eine einzelne Stoßwellenbehandlung zur Verbesserung des Knorpels und der subchondralen Knochenqualität führt.
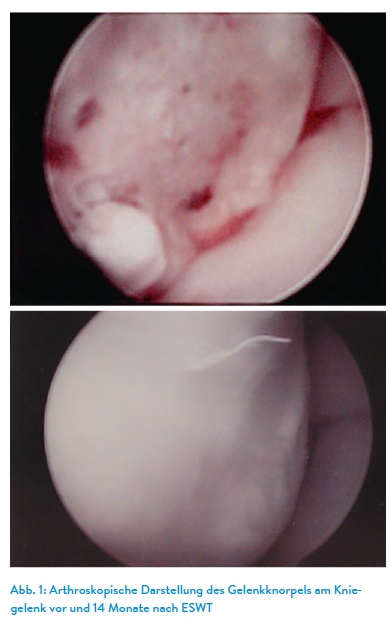
Im Jahr 2003 konnten wir14 in einer arthroskopisch kontrollierten Fallvorstellung eine regeneration der Knorpeloberfläche bei einem großflächigen Defekt im Bereich der medialen Femurkondyle durch eine direkte hochenergetische Stoßwellenbehandlung mit einem elektrohydraulischen Stoßwellengenerator bei 0,35 mJ/mm2 bei einem 29-jährigen Hobbysportler darstellen.
Die seit mehr als zwei Jahren bestehenden Beschwerden zeigten eine VAS-Reduktion von 7 auf 2 innerhalb von 2 Wochen und konnten im weiteren Beobachtungszeitpunkt nach 12, 26 und 52 Wochen sich stabil bei 0 halten. Diese Fallbeobachtung erfolgte im Rahmen einer Studie zur Untersuchung der ESWT bei Osteochondrosis dissecans.
In der Studie zur ESWT bei Osteochondrosis dissecans an Knie und Talus15 zeigte sich eine Regeneration der osteochondralen Läsion mit Score-Verbesserungen in der Beurteilung der MRT-Verlaufskontrolle sowie klinischen Scores. Zuletzt haben Cheng et al.16 eine Veröffentlichung zur ESWT bei osteochondralen Läsionen mit Untersuchung verschiedener Wachstumsfaktoren veröffentlicht. Es wurden die Effekte auf TGF-β, sowie BMP-2, -4, -5 und -7 untersucht. Wieder wurden 800 Impulse mit einer Energieflussdichte von 0,25 mJ/mm2 appliziert.
Neben den positiven Effekten auf Sehnen, Knochen und Muskulatur zeigt sich auch eine positive Wirkung auf den Gelenkknorpel. Die am betroffenen Gewebe applizierten energiereichen Stoßwellen zeigen Einfluss auf eine verbesserte Blutzufuhr, Aktivierung des zellulären Metabolismus und
Stimulation der Freisetzung von verschiedenen Wachstumsfaktoren. Die regenerativen Potentiale der Stoßwellentherapie am Gelenkknorpel liegen in:
- Stimulation der Kollagen-Produktion – ESWT kann die Synthese von Kollagen unterstützen und damit die Stabilität vom Gelenkknorpel verstärken und Knorpelschäden reparieren.
- Blutzufuhr v erbessern – Die Anwendung von Stoßwellen zeigt eine Dilatation von Blutgefäßen und Verbesserung des Blutflusses mit resultierender Verbesserung von Sauerstoff- und Nährstoffzufuhr, was bei der Heilung von Gelenkknorpel essenziell ist, der ja grundsätzlich bereits einen limitierten Blutfluss aufweist.
- Fördert die Zell-Regeneration – ESWT kann die Aktivität von Chondrozyten unterstützen, die für den Erhalt von Knorpelgewebe essenziell sind, womit eine Unterstützung der Heilung ermöglicht wird.
- Reduktion von Schmerz und Inflammation – über die Freisetzung von Endorphinen und Modulation von Entzündungsmediatoren wird eine Schmerzreduktion erzielt und die Schaffung einer regenerativen Umgebung erreicht.
|
Bereits nach 4 Wochen zeigte sich in der Behandlungsgruppe eine glattere Oberflächenstruktur des Knorpels, nach 12 Wochen zeigte sich eine vollständige Überziehung der Gelenkfläche mit dem Knorpelregenerat.
Interessanterweise konnte nachgewiesen werden, dass im Sinne einer regenerativen Veränderung, die Heilung charakterisiert war durch eine „bottom-to-top“ und „edge-to-center“ Veränderung, wie es für eine Regeneration aus dem gesunden Gewebe zu erwarten ist.
Die histologischen Untersuchungen zeigten weiter eine reduktion von fibrotischem Typ-1-Kollagen, während die expression von Typ-2-Kollagen gesteigert werden konnte durch Anwendung der ESWT. Hierfür spricht auch der signifikant höhere Nachweis von SOX9 und Aggrecan zwölf Wochen nach ESWT in der Behandlungsgruppe.
Die Konzentrationen von TGF-β und BMP zeigten einen positiven Einfluß auf die Chondrozytenproliferation und Knorpelneubildung.
Zusammenfassend konnte gezeigt werden, dass die in der humanmedizinischen Anwendung der extrakorporalen Stoßwellentherapie verwendeten Energieflussdichten keine zellschädigenden Wirkungen haben, sondern ein Auslöser für einen biologischen Effekt im behandelten Gewebe sind. Auch wenn nicht immer eine Verbesserung erwartet werden, kann, so kann in Bezug auf die Entwicklung der Arthrose aber neben der symptomatischen Verbesserung auch ein Aufhalten der fortschreitenden Verschlechterung erreicht werden.
ESWT in der aktuellen Behandlung:
Unter Berücksichtigung der aktuellen Studienlage zur Wirkung von ESWT auf subchondralen Knochen und Gelenkkorpel und Betrachtung der unterschiedlichen Ursachen für eine Knorpelschädigung lässt sich entsprechend der betroffenen Strukturen unterscheiden, wie und welche Struktur behandelt werden sollte. Es gilt zu unterscheiden, ob ein chondraler Defekt besteht, also die Läsion allein auf den Knorpel begrenzt ist, oder aber bei osteochondralen Defekten auch der subchondrale Knochen beteiligt ist. Auch sollten die Möglichkeiten einer regenerativen Behandlung mit Wiederherstellung der originalen Struktur des Gelenkknorpels von der reparierenden Defektheilung mit Bildung eines Ersatzknorpels minderwertiger Qualität beachtet werden.
Neben den positiven Effekten auf Knorpel und Knochenqualität sind aktuell gerade bei der Gonarthrose die symptomatischen Verbesserungen für die Patienten in den Vordergrund gerückt. Lu et al.17 zeigen in einer Metaanalyse einen signifikanten Effekt der Behandlung der Osteoarthrose in Bezug auf Schmerzreduktion und Funktionsverbesserung. Die Effekte zeigen eine Überlegenheit gegenüber Placebo, Hyaluronsäure, Kortikosteroide, NSAR, Ultraschall und PRP Lediglich Manuelle Therapie und operative Versorgungen zeigten vergleichbare Ergebnisse.
Regenerative Potentiale der extrakorporalen Stoßwellentherapie am Gelenkknorpel:
Bei der Behandlung einer Schädigung des Gelenkknorpels aufgrund einer reinen Veränderung des Knorpels scheint aktuell, angelehnt an die beschrieben mechanotransduktiven Effekte auf Gelenkknorpel, eine direkte Behandlung der Knorpeloberfläche mit einer niedrigen Energieflussdichten zu erfolgen, während bei der Behandlung des subchondralen Knochens für eine Veränderung der Gelenkoberfläche eine humanmedizinisch hochenergetische Intensität von 0,25 mJ/mm2 zur Anwendung kommt.
Neben der regenerativen Behandlung erfolgt aktuell häufig auch eine symptomatische Behandlung mit der Zielstellung den entzündlichen Prozess im Gelenk zu beeinflussen. Hierbei werden ebenfalls eher niedrige Energieflussdichten im Bereich der Gelenkkapsel zur Anwendung kommen. Es lassen sich drei wesentliche Aspekte unterscheiden in der Behandlung der Arthrose mittels ESWT, aber auch sonstigen Therapieformen. Hier sind drei Strukturen im Ziel der Behandlung. Das Knochenmarködem, die Synovialitis und der Gelenkknorpel. Im Gegensatz zu vielen anderen Therapieoptionen, die einzelne Targets ansprechen, um eine symptomatische und strukturelle Veränderung zu erzielen, kann die ESWT an allen drei Strukturen direkt zur Anwendung gebracht werden, um eine Schmerzreduktion und Funktionsverbesserung, aber eben auch eine strukturelle Verbesserung des Gelenkknorpels zu erreichen.
Literatur auf Anfrage bei der Redaktion.