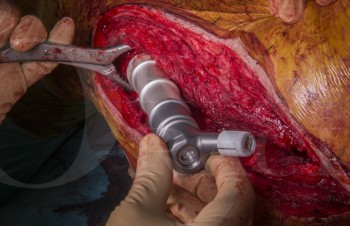
Die Zahl chirurgischer Eingriffe bei Patienten mit chronisch entzündlichen rheumatischen Erkrankungen steigt kontinuierlich – sei es aufgrund gelenkerhaltender Maßnahmen, endoprothetischer Versorgung oder traumatologischer Indikationen. Ein erheblicher Teil dieser Patienten steht unter immunsuppressiver Therapie, insbesondere mit Biologika oder konventionellen DMARDs. Diese Substanzen erhöhen das Risiko postoperativer Infektionen und beeinträchtigen die Wundheilung – gleichzeitig kann das Absetzen einen Schub der Grunderkrankung auslösen. Ziel dieses Artikels ist es, evidenzbasierte Empfehlungen zum perioperativen Management rheumatologischer Patienten unter Immunsuppression darzustellen und eine Empfehlung für die tägliche Praxis zu geben.
Grundlagen der Immunsuppression bei rheumatologischen Erkrankungen
Moderne Therapieansätze kombinieren konventionelle synthetische DMARDs (csDMARDs) wie Methotrexat oder Leflunomid mit Biologika (bDMARDs) oder zielgerichteten synthetischen DMARDs (tsDMARDs), z. B. JAK-Inhibitoren. Die Wirkung dieser Medikamente beruht auf einer Modulation der Immunantwort – sie reduzieren effektiv die Krankheitsaktivität, aber auch die Fähigkeit zur Infektabwehr. Häufig werden auch weiterhin Glukokortikoide als begleitende Therapie verabreicht, häufig in Kombination mit Immunsuppressiva, um die Wirkung zu verstärken beziehungsweise die Dosis zu verringern.
Immunsuppressiva im rheumatologischen Kontext

Infektionsrisiko und Wundheilung: Eine klinische Gratwanderung
Zahlreiche Studien belegen ein erhöhtes Risiko für postoperative Infektionen, insbesondere bei
- hoher Krankheitsaktivität
- gleichzeitiger Glukokortikoidgabe (> 5 mg Prednisonäquivalent)
- großen oder endoprothetischen Eingriffen
- komplexen Eingriffen an den Händen oder den Vorfüßen
- zusätzlicher Multimorbidität (z. B. Diabetes, Niereninsuffizienz).
Das Risiko einer perioperativen Infektion wird von einer Vielzahl von Faktoren beeinflusst. Insbesondere beim Rheumapatienten ist die komplexe Ausgangssituation zu berücksichtigen. Die Patienten haben wegen der Grunderkrankung ein per se erhöhtes Infektionsrisiko. Daher ist es im Vorfeld wichtig, dass der Patient bestmöglich medikamentös eingestellt ist. Zusätzlich kommen patientenbezogene Risikofaktoren wie Adipositas, Diabetes mellitus und andere Grunderkrankungen, die sich potentiell ungünstig auf das Operationsrisiko auswirken. Diese sollten präoperativ ebenfalls behandelt werden.
Bei endoprothetischen Eingriffen ist zusätzlich das erhöhte Osteoporose-Risiko zu beachten. Eine reduzierte Knochendichte kann sich negativ auf die Stabilität und auch die Prognose auswirken. Darüber hinaus ist eine genaue Anamnese vorausgegangener Infektionen wichtig, um Folgeinfektionen zu minimieren.
Spezielle Empfehlungen zu häufigen Medikamenten
Glukokortikoide
Häufig wird die Wertigkeit und auch das Risiko einer Cortisonbehandlung unterschätzt. Es besteht ein dosisabhängig zunehmendes Operationsrisiko für Infektionen. Daher ist die tägliche Steroiddosis möglichst zu senken; Ziel ist ein Prednisolonäquivalent unter 5 mg pro Tag. Im Idealfall wird die Medikation gänzlich abgesetzt. Eine Dosissteigerung vor dem Hintergrund einer perioperativen hormonellen Instabilität, bedingt durch den operativen Stress und eine Nebenniereninsuffizienz, ist nicht erforderlich.
Methotrexat (MTX)
MTX ist das häufigste Basismedikament. Es wird einmal wöchentlich subkutan oder oral eingenommen. In der Vergangenheit haben sich keine Hinweise ergeben, dass für Patienten, die MTX einnehmen, ein erhöhtes postoperatives Komplikationsrisiko besteht, daher kann die Therapie fortgeführt werden. Lediglich bei Patienten mit einer entsprechenden Medikation sollte im Hinblick auf die hepatische Verstoffwechselung gegebenenfalls erwogen werden, eine einwöchige Pause durchzuführen.
Leflunomid
Leflunomid wird täglich in einer Dosis von 10–20 mg oral verabreicht. Die Halbwertszeit liegt bei vier Wochen; der aktive Metabolit Teriflunomid verbleibt aber wegen der komplexen enterohepatischen Rezirkulation zwei Jahre im Körper. Ein kurzfristiges Absetzen ist daher nicht sinnvoll. Bei einem erhöhten Infektionsrisiko kann das Auswaschen zur beschleunigten Elimination durchgeführt werden. Sowohl nach Empfehlungen der DGRh als auch der ACR-Leitlinie kann die Therapie bei niedrigem Risiko fortgeführt werden. Vereinzelt kam es auf Kongressen zu Berichten von erheblichen Wundheilungsstörungen, insbesondere bei Operationen an den kleinen Gelenken an den Händen oder Füßen. Hier sollte gegebenenfalls nach Rücksprache mit dem Operateur tatsächlich empfohlen werden, die Medikation auszuwaschen. Die Empfehlung dafür ist der Einsatz von 8 mg Colestyramin dreimal täglich für 5–8 Tage oder 50 mg Aktivkohle viermal täglich über fünf Tage. Anzumerken ist, dass beide Verfahren teilweise zu erheblichen Nebenwirkungen führen und von den Patienten nur sehr ungern durchgeführt werden.
Sulfasalazin
Grundsätzlich gilt auch hier, dass die Medikation fortgeführt werden sollte. Lediglich bei Patienten mit hepatischen Vorerkrankungen ist gegebenenfalls eine kurzfristige präoperative Pause begründet.
TNF-alpha Blocker
TNF-Inhibitoren werden mittlerweile häufig und auch sehr erfolgreich bei Patienten mit rheumatischen Erkrankungen eingesetzt. Die Datenlage hinsichtlich der Frage, wann diese Medikamente präoperativ abgesetzt werden sollten, ist relativ uneinheitlich. Allerdings kann mittlerweile nicht mehr davon ausgegangen werden, dass eine laufende TNF-Therapie das perioperative Risiko erhöht. Auf der anderen Seite gibt es Studien, die das Risiko für Flares bei zu langer Pause erfasst haben, die jeweils eine beträchtliche Steigerung des Risikos gesehen haben. Vor diesem Hintergrund ist es nicht mehr gerechtfertigt, weiterhin das Absetzen über einen Zeitraum von zwei Halbwertszeiten zu fordern. Die Empfehlung lautet daher, die Therapiepause auf eine Halbwertszeit zu verkürzen, d. h. in der Regel eine Applikation präoperativ auszusetzen oder aber, falls dies möglich ist, die Operation am Ende des Therapieintervalls durchzuführen.
Azathioprin, Ciclosporin A und Mycophenolat
Die immunsuppressiven Wirkstoffe Azathioprin, Ciclosporin A und Mycophenolat werden vor allem bei Patienten mit schweren systemischen Autoimmunerkrankungen wie Kollagenosen (z. B. systemischer Lupus erythematodes) oder Vaskulitiden eingesetzt. Trotz ihrer breiten Anwendung ist die Studienlage zur perioperativen Handhabung dieser Substanzen bislang unzureichend für evidenzbasierte Empfehlungen. In den ACR-Leitlinien wird empfohlen, die Therapie bei Patienten mit aktiver, schwerer Grunderkrankung fortzuführen, da das Risiko eines Krankheitsrückfalls durch ein Absetzen der Medikation höher eingeschätzt wird als das perioperative Infektionsrisiko.
Für Operateure besonders relevant: Alle drei Medikamente haben kurze Halbwertszeiten (Azathioprin: 4–5 h, Ciclosporin A: 5–10 h, Mycophenolat: ca. 16 h). Eine kurzfristige Pause von 1–2 Tagen vor einem elektiven Eingriff führt in der Regel zu keiner signifikanten Beeinflussung des perioperativen Verlaufs. Die immunsuppressive Wirkung kann zwar über diesen Zeitraum hinaus bestehen, klinisch relevante Auswirkungen auf die Wundheilung oder Infektionsrate sind bei kurzer Unterbrechung jedoch nicht zu erwarten. Gleichzeitig bleibt das Risiko eines rheumatischen Schubs bei dieser Vorgehensweise gering. Eine Weiterführung der genannten Immunsuppressiva ist bei stabiler Krankheitskontrolle in der Regel möglich.
Abatacept
Aktuelle Studien geben keinen Hinweis, dass eine Pausierung von Abatacept die perioperativen Komplikationen reduziert. Die OP-Planung sollte, wenn dies möglich ist, so durchgeführt werden, dass die Operation am Ende des Therapieintervalls durchgeführt wird.
Rituximab
Für die B-Zell-Depletion mit Rituximab liegt ebenfalls nur eine unzureichende Datenlage vor. Allerdings wird zusammenfassend empfohlen, elektive Eingriffe vier Monate nach der letzten Infusion und spätestens vier Wochen vor der nächsten Infusion zu planen. Niedrige Immunglobulin-Spiegel können das Infektionsrisiko erhöhen; daher könnte eine präoperative Bestimmung des Immunglobulin-Spiegels, insbesondere bei einem erhöhten Infektionsrisiko oder bei wiederkehrenden Infektionen, sinnvoll sein. Gegebenenfalls besteht auch die Indikation für eine Substitution.
Interleukin-6-Rezeptor Inhibitoren
In dieser Gruppe ist es wichtig zu beachten, dass Tocilizumab die Warnsignale einer postoperativen Infektion unterdrückt. Bakterielle Infektionen können maskiert werden, es besteht kein Anstieg der Entzündungsparameter (CRP, Fieber). Zusammenfassend ist die Empfehlung jedoch, Tocilizumab und Sarilumab analog der übrigen bDMARDs operativ zu pausieren.
Interleukin-1, 17, 12/23 und 23 Inhibitoren
Für die Interleukin-Inhibitoren Anakinra, Canakinumab, Ixekizumab, Secukinumab, Guselkumab und Ustekinumab und auch für den (BLyS)-Inhibitor Belimumab besteht die gleiche Empfehlung wie oben. Auch hier wird empfohlen, analog zu den anderen bDMARDs die geplante Operation zum Ende des jeweiligen Therapieintervalls festzusetzen. Da Anakinra eine sehr kurze Halbwertszeit (4–6 h) hat, ist hier eine Pause 1–2 Tage vor der OP ausreichend.
Targeted-synthetic DMARDs
Zu der Gruppe der tsDMARDs oder auch „small molecules“ zählen ein Phosphodiesterase 4 (PDE4)-Inhibitor (Apremilast) und vier Januskinase (JAK)-Inhibitoren (Baricitinib, Filgotinib, Tofacitinib, Upadacitinib), die oral verabreicht werden und alle eine kurze Halbwertszeit (3–max. 14 h) haben. Dies bedeutet, dass diese Substanzen gut steuerbar sind. Daher reicht eine drei- bis viertägige Pause präoperativ aus. Nach Expertenmeinung der DGRh kann Apremilast perioperativ fortgeführt werden. Alle tsDMARDs sollten baldmöglichst bei regelrechten Wundverhältnissen wieder begonnen werden. Wegen der kurzen Halbwertszeit sollte die Therapie innerhalb von 3–5 Tagen wieder fortgesetzt werden. Wenige Tage der Unterbrechung können bereits einen Schub auslösen. Eine Pause von mehr als 14 Tagen sollte perioperativ nicht überschritten werden.
Empfehlung zu den einzelnen Substanzen – für die Praxis
Glukokortikoide
Evidenzlage:
Mehrere große, retrospektive Studien zeigen ein dosisabhängig erhöhtes Risiko für postoperative Infektionen, Mortalität und Re-Hospitalisierung, insbesondere ab >10 mg Prednisolonäquivalent/Tag.
Empfehlung für die chirurgische Praxis:
→ Ziel: GC-Dosis <5 mg/Tag in den 3 Monaten vor elektiven OPs
→ Keine kurzfristige Reduktion vor OP notwendig
→ Am OP-Tag: übliche Tagesdosis verabreichen – keine zusätzliche „Stressdosis“ notwendig bis 20 mg/Tag
Methotrexat (MTX)
Evidenzlage:
RCTs zeigen kein erhöhtes perioperatives Risiko – bei RA und CED sogar möglicherweise protektiv. Keine Daten zu Dosen >20 mg/Woche.
Empfehlung für die chirurgische Praxis:
→ Therapie kann fortgeführt werden
→ Bei Hochdosis (>20 mg/Woche) evtl. Reduktion auf ≤15 mg/Woche
→ Injektionszeitpunkt bei Bedenken verschieben
Leflunomid
Evidenzlage:
Uneinheitliche Studienlage – einzelne Hinweise auf Wundheilungsstörungen. Lange HWZ (bis 2 Jahre) durch enterohepatische Rezirkulation.
Empfehlung für die chirurgische Praxis:
→ Kleine OPs, geringes Risiko: Fortführung möglich (cave bei Eingriffen an Händen und Füßen)
→ Größere Eingriffe: Auswaschung (z. B. mit Cholestyramin)
→ Einfaches Absetzen ohne Auswaschung ist nicht sinnvoll
Sulfasalazin
Evidenzlage:
Keine erhöhte Infektionsrate – möglicherweise sogar protektiver Effekt. Kurze HWZ (6–8 h).
Empfehlung für die chirurgische Praxis:
→ Kann fortgeführt werden
→ Bei Bedenken: Absetzen am Vortag, Wiederbeginn postoperativ
Hydroxychloroquin
Evidenzlage:
Keine Hinweise auf erhöhtes Risiko. Lange HWZ (40–50 Tage). Kein signifikanter immunmodulierender Effekt.
Empfehlung für die chirurgische Praxis:
→ Fortführen empfohlen
→ Kurzfristige Pause möglich – ohne Risiko für Krankheitsschub
Azathioprin, Ciclosporin A, Mycophenolat
Evidenzlage:
Keine Studien – Empfehlungen basieren auf Expertenmeinung und ACR-Stratifizierung nach Krankheitsaktivität.
Empfehlung für die chirurgische Praxis:
→ Kurze Pause (1–2 Tage) möglich, aber nicht zwingend notwendig
→ Bei aktiver Erkrankung: Therapie fortsetzen in Absprache mit Rheumatologen
TNF-Inhibitoren (z. B. Infliximab, Adalimumab, Etanercept)
Evidenzlage:
Heterogene Datenlage. Metaanalysen zeigen teils leicht erhöhtes Risiko bei Fortführung, aber auch erhöhtes Schubrisiko bei zu langer Pause. Kein Vorteil längerer Absetzphasen.
Empfehlung für die chirurgische Praxis:
→ Pause von einem Dosierungsintervall (nicht mehr zwei HWZ)
→ Balance zwischen Infektions- und Schubrisiko beachten
Abatacept
Evidenzlage:
Drei Studien zeigen keinen Vorteil längerer Pausen. Komplikationsraten unabhängig von Pause oder Applikationsform.
Empfehlung für die chirurgische Praxis:
→ OP-Termin am Ende des Therapieintervalls
→ Keine verlängerte Pause notwendig
Rituximab
Evidenzlage:
Nur eine retrospektive Kohorte mit begrenzter Aussagekraft. Infektionsrisiko möglicherweise abhängig von IgG-Spiegel.
Empfehlung für die chirurgische Praxis:
→ OP idealerweise 4 Monate nach letzter Infusion
→ Bei hohem Risiko: präoperative IgG-Kontrolle, ggf. Substitution vor OP
IL-6-Inhibitoren (z. B. Tocilizumab, Sarilumab)
Evidenzlage:
Kein Zusammenhang zwischen Komplikationen und Infusionszeitpunkt. Tocilizumab maskiert Infektionszeichen (Fieber, CRP).
Empfehlung für die chirurgische Praxis:
→ Pause von einem Dosierungsintervall empfohlen
→ Wachsamkeit bei Infektionsdiagnostik nötig
Interleukin-Inhibitoren (IL-1, IL-17, IL-12/23, IL-23)
Evidenzlage:
Keine relevanten Studiendaten verfügbar.
Empfehlung für die chirurgische Praxis:
→ OP am Ende des Therapieintervalls planen
→ Anakinra: kurze HWZ → 1–2 Tage Pause ausreichend
tsDMARDs (JAK-Inhibitoren, Apremilast)
Evidenzlage:
Wenig Daten, z. T. erhöhte Infektions- und VTE-Raten. Kurze HWZ.
Empfehlung für die chirurgische Praxis:
→ Pause: 3–4 Tage vor OP, Wiedereinleitung bei regelrechter Wundheilung
→ Maximale Pause 14 Tage, um Schübe zu vermeiden
→ Apremilast: Fortführung möglich, Pause optional

Fallbeispiel
Ein 64-jähriger Patient mit rheumatoider Arthritis unter Methotrexat (15 mg/Woche) und Adalimumab (alle 2 Wochen), zusätzlich Prednisolon 5 mg/Tag, wird elektiv zur Hüfttotalendoprothese aufgenommen.
Empfehlung:
→ Adalimumab pausieren – letzter Pen 2 Wochen vor OP
→ Methotrexat beibehalten
→ Glukokortikoide: 5 mg/Tag fortführen
→ Biologikum wieder aufnehmen nach 14 Tagen bei reizloser Wunde
Postoperativer Verlauf komplikationslos. Entlassung am Tag 7, Biologikatherapie Wiederbeginn in Woche 3.
Fazit
Das perioperative Management rheumatologischer Patienten unter Immunsuppression erfordert eine differenzierte, individuelle Planung. Während Biologika je nach Substanz vorübergehend pausiert werden sollten, können konventionelle DMARDs oft weitergeführt werden. Die enge Zusammenarbeit aller beteiligten Fachrichtungen ist essenziell, um die Balance zwischen Infektionsschutz und Krankheitskontrolle zu wahren.
Abschließend noch ein Hinweis: wichtig ist die Wiederaufnahme der Basistherapie postoperativ. Dies wird in der Praxis leider immer wieder vergessen, insbesondere wenn der Patient nicht in einer spezialisierten Klinik behandelt wurde oder in der Nachbehandlung nicht auf die Medikation geachtet wurde.
Literatur
- Schweizerische Gesellschaft für Rheumatologie (SGR). Perioperatives Management von Basistherapeutika. Version 2022.
- Goodman SM et al. ACR/AAHKS Guidelines for Perioperative Management of Antirheumatic Medication. Arthritis Care Res. 2022.
- EULAR Recommendations for the Management of Rheumatoid Arthritis. Ann Rheum Dis. 2019.
- RKI Impfempfehlungen für Immunsupprimierte. Stand 2023.
- Ravi B et al. Impact of Biologic DMARDs on Surgical Outcomes. J Bone Joint Surg Am. 2022.
- Krüger, Klaus et al. Perioperativer Umgang mit der Therapie von Patienten mit entzündlich- rheumatischen Erkrankungen, Aktualisierte Empfehlungen der DGRh, Erstveröffentlichung, Januar 2022 / zuletzt überprüft August 2024