Würzburg – Bei der Suche nach verbesserten Medikamenten zur Behandlung der Knochenkrankheit Osteoporose setzt die Forschung unter anderem auf das Protein Sclerostin, das im Knochenstoffwechsel eine Rolle spielt. Hemmt man seine Funktion, wird der Knochenabbau unterdrückt. Würzburger Forscher haben nun erstmals einen gegen Sclerostin wirksamen Antikörper in kristalliner Form dargestellt und seine Wirkungsweise analysiert.
Erste klinische Studien mit einem Sclerostin-hemmenden Antikörper der Firmen Amgen und UCB zeigten eine Zunahme der Knochenmasse bei Osteoporose-Patienten. Aktuell laufen weiterführende Studien unter anderem in Würzburg, München und Dresden.
Suche nach neuen Antikörpern
In einem von der Europäischen Union und der Deutschen Forschungsgemeinschaft geförderten Projekt arbeiten Würzburger Wissenschaftler gemeinsam mit weiteren Projektpartnern daran, neue Antikörper zu erzeugen, die sich gegen Sclerostin richten.
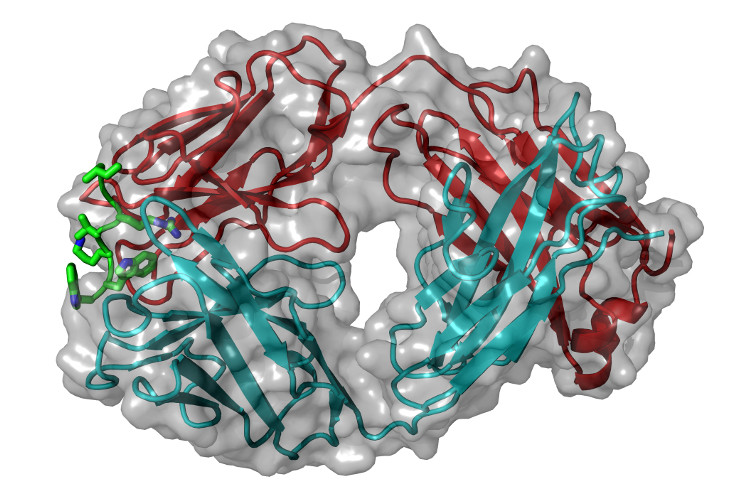
Dabei haben die Forscher nun erstmals einen gegen Sclerostin wirksamen Antikörper in kristalliner Form dargestellt und seine Wirkungsweise genauer analysiert. „Sie könnten das Design neuer, hochwirksamer Antikörper gegen Sclerostin vorwärts bringen”, so Dr. Verena Boschert vom Julius-von-Sachs-Institut der Universität Würzburg.
Zusammenarbeit mit der Industrie
Die Würzburger Forscher kooperieren bei diesen Arbeiten mit der Industrie. Gemeinsam mit der Firma AbD Serotec, die ihre deutsche Niederlassung in Puchheim hat, wurden zuerst rund zehn Antikörper entwickelt, die vielversprechend schienen. In Zellkulturen zeigte sich dann, dass genau einer davon gegen Sclerostin wirksam ist.
Gemeinsam mit dem niederländischen Unternehmen Pepscan und dem Leibniz-Institut für molekulare Pharmakologie in Berlin wurden außerdem ein sogenanntes Epitop-Mapping und NMR-Studien durchgeführt. Diese Analysenmethoden brachten zutage, an welcher Stelle genau sich der Antikörper an Sclerostin heftet.
Die nächsten Forschungsschritte
„Bislang haben wir nur den Antikörper kristallisiert und untersucht“, sagt Boschert. Als nächstes ist nun geplant, den Antikörper gemeinsam mit dem Abschnitt von Sclerostin zu kristallisieren, an den er bindet. Auf diese Weise sollten sich noch detailliertere Informationen über die Art und Weise der Bindung gewinnen lassen.
Die Ergebnisse der Forscher wurden am 24. August online unter dem Titel „The sclerostin-neutralizing antibody AbD09097 recognizes an epitope adjacent to sclerostin’s binding site for the Wnt co-receptor LRP6“ in der Fachzeitschrift Open Biology veröffentlicht.
Quelle: Julius-Maximilians-Universität Würzburg